Валодаючы асаблівымі фізічнымі і хімічнымі ўласцівасцямі, каалін з'яўляецца незаменным неметалічным мінеральным рэсурсам у вытворчасці керамікі, паперы, гумы, пластмас, вогнеўпораў, нафтаперапрацоўкі і іншых прамысловых, сельскагаспадарчых і абаронных галінах перадавых тэхналогій. Беласць кааліну - важны паказчык яго прымянення.

Фактары, якія ўплываюць на беласць кааліну
Каалін - гэта разнавіднасць дробназярністай гліны або гліністай пароды, якая ў асноўным складаецца з мінералаў каалініту. Яго крышталёвая хімічная формула 2SiO2 · Al2O3 · 2H2O. Невялікую колькасць негліністых мінералаў складаюць кварц, палявы шпат, мінералы жалеза, тытана, гідраксід і аксіды алюмінію, арганічныя рэчывы і інш.
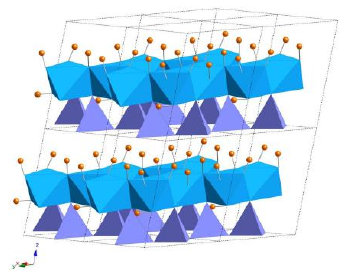
Крышталічная структура кааліну
У адпаведнасці са станам і прыродай прымешак у кааліне, прымешкі, якія выклікаюць памяншэнне беласці кааліну, можна падзяліць на тры катэгорыі: арганічны вуглярод; Пігментныя элементы, такія як Fe, Ti, V, Cr, Cu, Mn і г.д.; Цёмныя мінералы, такія як біятыт, хларыт і інш. Як правіла, утрыманне V, Cr, Cu, Mn і іншых элементаў у кааліне невялікае, што мала ўплывае на беласць. Мінеральны склад і ўтрыманне жалеза і тытана - асноўныя фактары, якія ўплываюць на беласць кааліну. Іх існаванне паўплывае не толькі на натуральную беласць кааліну, але і на яго кальцыніраванай беласць. У прыватнасці, наяўнасць аксіду жалеза негатыўна адбіваецца на колеры гліны і зніжае яе яркасць і вогнеўстойлівасць. І нават калі колькасць аксіду, гідраксіду і гідратнага аксіду аксіду жалеза складае 0,4%, гэтага дастаткова для надання гліністаму асадку чырвонай да жоўтай афарбоўкі. Гэтымі аксідамі і гідраксідамі жалеза могуць быць гематыт (чырвоны), маггеміт (чырвона-карычневы), гетыт (карычнева-жоўты), ліманіт (аранжавы), гідратаваны аксід жалеза (карычнева-чырвоны) і г. д. Можна сказаць, што выдаленне прымешак жалеза у кааліну гуляе надзвычай важную ролю ў больш эфектыўным выкарыстанні кааліну.
Стан узнікнення элемента жалеза
Ступень прысутнасці жалеза ў кааліне з'яўляецца асноўным фактарам, які вызначае спосаб абезжалезвання. Вялікая колькасць даследаванняў мяркуе, што крышталічнае жалеза ў выглядзе дробных часціц змешваецца ў кааліне, у той час як аморфнае жалеза пакрываецца на паверхні дробных часціц кааліну. У цяперашні час стан прысутнасці жалеза ў кааліне дзеліцца на два тыпу ў краіне і за мяжой: адзін - у каалініце і дадатковых мінералах (такіх як лушчак, дыяксід тытана і іліт), які называецца канструкцыйным жалезам; Іншы знаходзіцца ў выглядзе самастойных мінералаў жалеза, званых свабодным жалезам (уключаючы жалеза на паверхні, дробназярністае крышталічнае жалеза і аморфнае жалеза).

Жалеза, выдаленае шляхам абезжалезвання і адбельвання кааліну, з'яўляецца свабодным жалезам, у асноўным уключаючы магнетыт, гематыт, ліманіт, сідэрыт, пірыт, ільменіт, яразіт і іншыя мінералы; Большая частка жалеза існуе ў выглядзе высокадысперснага калоіднага ліманіту і невялікая колькасць у форме сферычнага, ігольчастага і няправільнага гетыта і гематыту.
Метад абезжалезвання і адбельвання кааліну
Аддзяленне вады
Гэты метад у асноўным выкарыстоўваецца для выдалення абломкавых мінералаў, такіх як кварц, палявы шпат і лушчак, і больш грубых прымешак, такіх як абломкі горных парод, а таксама некаторых мінералаў жалеза і тытана. Мінералы-прымешкі з такой жа шчыльнасцю і растваральнасцю, як каалін, не могуць быць выдалены, а паляпшэнне беласці адносна невідавочнае, што падыходзіць для ўзбагачэння і адбельвання адносна высакаякаснай каалінавай руды.
Магнітная сепарацыя
Мінеральныя прымешкі жалеза ў кааліне звычайна слабамагнітныя. У цяперашні час у асноўным выкарыстоўваецца метад моцнай магнітнай сепарацыі з высокім градыентам, альбо слабыя магнітныя мінералы пасля абпалу пераўтвараюцца ў моцнамагнітны аксід жалеза, а затым выдаляюцца звычайным метадам магнітнай сепарацыі.

Вертыкальны кальцавой магнітны сепаратар з высокім градыентам

Высокаградыентны магнітны сепаратар для электрамагнітнай суспензіі

Нізкотэмпературны звышправодны магнітны сепаратар
Метад флотации
Для ачысткі кааліну першасных і другасных радовішчаў выкарыстоўваецца метад флотации. У працэсе флотации часціцы каалініту і лушчака аддзяляюцца, а вычышчаныя прадукты з'яўляюцца некалькімі прыдатнымі сыравінай прамысловага класа. Селектыўнае флотационное падзел каалініту і палявога шпата звычайна праводзіцца ў шламе з кантраляваным рн.
Метад скарачэння
Метад аднаўлення заключаецца ў выкарыстанні аднаўляльніка для аднаўлення прымешак жалеза (такіх як гематыт і ліманіт) у трохвалентным стане кааліну да растваральных іёнаў двухвалентнага жалеза, якія выдаляюцца шляхам фільтрацыі і прамывання. Выдаленне прымешак Fe3+ з прамысловага кааліну звычайна дасягаецца спалучэннем фізічных тэхналогій (магнітная сепарацыя, селектыўная флокуляцыя) і хімічнай апрацоўкі ў кіслотных або аднаўленчых умовах.
Гідрасульфіт натрыю (Na2S2O4), таксама вядомы як гідрасульфіт натрыю, эфектыўны пры аднаўленні і вымыванні жалеза з кааліну і ў цяперашні час выкарыстоўваецца ў каалінавай прамысловасці. Аднак гэты метад павінен праводзіцца ў моцных кіслотных умовах (pH<3), што прыводзіць да высокіх эксплуатацыйных выдаткаў і ўздзеяння на навакольнае асяроддзе. Акрамя таго, хімічныя ўласцівасці гідрасульфіту натрыю нестабільныя, што патрабуе спецыяльных і дарагіх механізмаў захоўвання і транспарціроўкі.
Дыяксід тиомочевины: (NH2) 2CSO2, TD) з'яўляецца моцным аднаўляльнікам, які мае такія перавагі, як моцная аднаўленчая здольнасць, экалагічнасць, нізкая хуткасць раскладання, бяспека і нізкі кошт серыйнай вытворчасці. Нерастваральны Fe3+у кааліне можа быць адноўлены да растваральнага Fe2+ праз TD.
У далейшым беласць кааліну можа быць павялічана пасля фільтрацыі і прамывання. TD вельмі стабільны пры пакаёвай тэмпературы і нейтральных умовах. Моцная аднаўленчая здольнасць TD можа быць атрымана толькі ва ўмовах моцнай шчолачнасці (pH>10) або нагрэву (T>70 °C), што прыводзіць да высокіх эксплуатацыйных выдаткаў і складанасці.
Метад акіслення
Акісленне ўключае выкарыстанне азону, перакісу вадароду, марганцоўкі і гіпахларыту натрыю для выдалення адсарбаванага вугляроднага пласта для паляпшэння беласці. Каалін у больш глыбокім месцы пад большай тоўшчай раскрышы мае шэры колер, а жалеза ў кааліне знаходзіцца ў аднаўленчым стане. Выкарыстоўвайце моцныя акісляльнікі, такія як азон або гіпахларыт натрыю, каб акісліць нерастваральны FeS2 у пірыце да растваральнага Fe2+, а затым прамыйце, каб выдаліць Fe2+ з сістэмы.
Метад кіслотнага вылугавання
Метад кіслотнага вылугавання заключаецца ў пераўтварэнні нерастваральных прымешак жалеза ў кааліне ў рэчывы, растваральныя ў кіслых растворах (салянай кіслаце, сернай кіслаце, шчаўевай кіслаце і г.д.), такім чынам ажыццяўляючы аддзяленне ад кааліну. У параўнанні з іншымі арганічнымі кіслотамі шчаўевая кіслата лічыцца найбольш перспектыўнай з-за яе кіслотнай сілы, добрай комплексаўтваральнай здольнасці і высокай аднаўленчай здольнасці. Са шчаўевай кіслатой растворанае жалеза можа быць асаджана з раствора для вымывання ў выглядзе оксалата двухвалентнага жалеза і можа быць дадаткова апрацавана з адукацыяй чыстага гематыту шляхам кальцынацыі. Шчаўевую кіслату можна танна атрымаць з іншых прамысловых працэсаў, а на стадыі абпалу пры вырабе керамікі любы рэшткавы оксалат у апрацаваным матэрыяле будзе раскладацца на вуглякіслы газ. Многія даследчыкі вывучалі вынікі растварэння аксіду жалеза шчаўевай кіслатой.
Метад высокатэмпературнага абпалу
Абпал - гэта працэс вытворчасці кааліну спецыяльнага гатунку. У залежнасці ад тэмпературы апрацоўкі вырабляюць дзве розныя маркі кальцыніраванага кааліну. Абпал у тэмпературным дыяпазоне 650-700 ℃ выдаляе структурную гідраксільную групу, а вылучаемы вадзяной пар павышае эластычнасць і непразрыстасць кааліну, што з'яўляецца ідэальным атрыбутам для нанясення пакрыцця на паперу. Акрамя таго, награваючы каалін пры тэмпературы 1000-1050 ℃, можна не толькі павялічыць сціральнасць, але і атрымаць 92-95% беласці.
Абпал хлараваннем
Жалеза і тытан былі выдалены з гліністых мінералаў, асабліва кааліну, шляхам хларавання, і былі атрыманы добрыя вынікі. У працэсе хларавання і абпалу пры высокай тэмпературы (700 ℃ - 1000 ℃) каалініт дэгідраксілюецца з адукацыяй метакаалініту, а пры больш высокай тэмпературы ўтвараюцца фазы шпінелі і муліту. Гэтыя пераўтварэнні павялічваюць гідрафобнасць, цвёрдасць і памер часціц шляхам спякання. Мінералы, апрацаваныя такім чынам, можна выкарыстоўваць у многіх галінах прамысловасці, такіх як папера, ПВХ, гума, пластмасы, клеі, паліроўка і зубная паста. Больш высокая гідрафобнасць робіць гэтыя мінералы больш сумяшчальнымі з арганічнымі сістэмамі.
Мікрабіялагічны метад
Тэхналогія мікробнай ачысткі мінералаў з'яўляецца адносна новай тэмай перапрацоўкі карысных выкапняў, уключаючы тэхналогію мікробнага вылугавання і тэхналогію мікробнай флотации. Тэхналогія мікробнага вылугавання мінералаў - гэта тэхналогія экстракцыі, якая выкарыстоўвае глыбокае ўзаемадзеянне паміж мікраарганізмамі і мінераламі для разбурэння крышталічнай рашоткі мінералаў і растварэння карысных кампанентаў. Акіслены пірыт і іншыя сульфідныя руды, якія змяшчаюцца ў кааліне, можна ачысціць з дапамогай тэхналогіі экстракцыі мікробаў. Звычайна выкарыстоўваюцца мікраарганізмы ўключаюць Thiobacillus ferrooxidans і Fe-аднаўляючыя бактэрыі. Мікрабіялагічны метад мае нізкі кошт і нізкае забруджванне навакольнага асяроддзя, што не паўплывае на фізічныя і хімічныя ўласцівасці кааліну. Гэта новы метад ачысткі і адбельвання з перспектывамі развіцця мінералаў кааліну.
Рэзюмэ
Апрацоўка кааліну для выдалення жалеза і адбельвання павінна выбраць найлепшы метад у залежнасці ад розных прычын афарбоўвання і розных задач прымянення, палепшыць комплексныя паказчыкі беласці мінералаў кааліну і зрабіць яго высокім спажывальным і эканамічным значэннем. Будучая тэндэнцыя развіцця павінна заключацца ў арганічным спалучэнні характарыстык хімічнага метаду, фізічнага метаду і мікрабіялагічнага метаду, каб у поўнай меры раскрыць іх перавагі і стрымаць іх недахопы і недахопы, каб дасягнуць лепшага эфекту адбельвання. У той жа час таксама неабходна далейшае вывучэнне новага механізму розных метадаў выдалення прымешак і ўдасканаленне працэсу, каб прымусіць выдаленне жалеза і адбельванне кааліну развівацца ў напрамку зялёнага, эфектыўнага і нізкавугляроднага.
Час публікацыі: 2 сакавіка 2023 г

