【Энцыклапедыя перапрацоўкі карысных выкапняў Huate】Фіялетавы выскачка! Huate Magneto Power спрыяе высакаякаснаму развіццю індустрыялізаванай вытворчай лініі для сартавання флюорыту
Флюарыт, таксама вядомы як флюарыт, багаты ітрыем, які называецца флюарытам ітрыю. Крышталі часта бываюць кубічнай формы, актаэдра і радзей рамбічнага дванаццацігранніка. Распаўсюджаны ў прыродзе мінерал, некаторыя ўзоры могуць выпраменьваць святло пры трэнні, награванні, ультрафіялетавым выпраменьванні і г. д. Яго рэдка выкарыстоўваюць у якасці каштоўных камянёў з-за яго далікатнасці і мяккасці. У прамысловасці флюарыт з'яўляецца асноўнай крыніцай для здабычы і атрымання розных злучэнняў, такіх як фтор і плавікавая кіслата, а ўзоры флюарыту з яркімі колерамі і прыгожымі формамі крышталяў могуць быць выкарыстаны для калекцыянавання, упрыгожвання і мастацтва разьбы.
Уласцівасці руды і будова мінерала
Флюарыт складаецца з CaF2, які змяшчае 48,67% фтору, 51,33% кальцыя і часам рэдкія элементы. Ён часта знаходзіцца ў сімбіёце з кварцам, кальцытам, барытам і сульфідам металу ў крупчастых або масіўных агрэгатах, часта жоўтых і зялёных. , сіні, фіялетавы і інш., менш бескаляровы, шклопадобны бляск, цвёрдасць 4, шчыльнасць 3,18 г/см3, награваецца або флуоресцентный пад ультрафіялетавым святлом. Флюарыт не раствараецца ў вадзе, раствараецца ў сернай кіслаце, фосфарнай кіслаце і гарачай салянай кіслаце, борнай кіслаце, хлорнаватай кіслаце і можа нязначна ўступаць у рэакцыю з моцнымі асновамі, такімі як гідраксід калію і гідраксід натрыю, з тэмпературай плаўлення 1360 °C.
Вобласці прымянення і тэхнічныя паказчыкі
Флюарыт змяшчае галагенавы элемент фтор, які з'яўляецца асноўнай сыравінай для атрымання злучэнняў фтору і шырока выкарыстоўваецца ў сталеліцейнай вытворчасці, выплаўцы каляровых металаў, вытворчасці цэменту, шкла, керамікі і інш., дзякуючы нізкай тэмпературы плаўлення. Даступны ў выглядзе аптычнага і рамеснага флюарыту.
Табліца 1 Асноўныя сферы выкарыстання флюарыту
| Поле прымянення | Асноўнае прызначэнне |
| Металургічная прамысловасць | Сталеплавільны флюс, шлакоудалитель, адбельвальнік эмалі, замутнитель шкла |
| Хімічная прамысловасць | Сыравіна для вытворчасці плавікавай кіслаты, асноўная сыравіна тыпу фрэону |
| Цэментная прамысловасць | Мінералізатар для вытворчасці цэментавага клінкеру, які дазваляе знізіць тэмпературу спякання і зэканоміць энергію |
| Шкляная прамысловасць | Сыравіна для вытворчасці эмульгаванага шкла, непразрыстага і таніраванага шкла, лінзаў |
| Керамічная прамысловасць | Растваральнікі і замутнільнікі для вырабу керамікі, эмалевых працэсаў |
Патрабаванні да тэхнічнага індэкса
Стандарты металургічнай прамысловасці дзеляць флюарытавую прадукцыю на тры тыпы: флюарытавы канцэнтрат (FC), флюарытавы кавалак (FL) і флюарытавую дробку (FF).
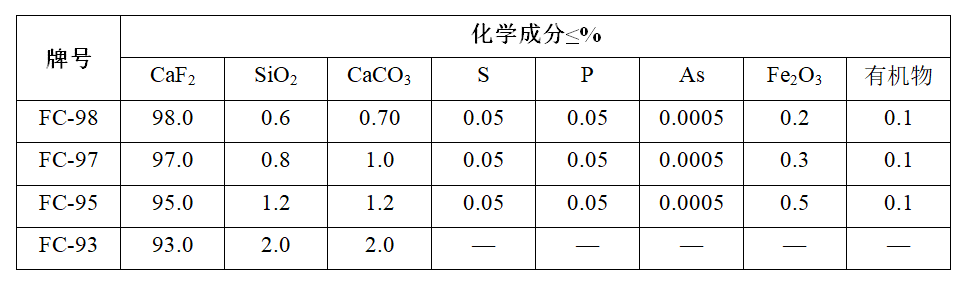
Табліца 2 Хімічны склад флюоритового канцэнтрату
Тэхналогія апрацоўкі
Ўзбагачэнне і ачыстка
Сімбіётамі з флюарытам з'яўляюцца мінералы: кварц, кальцыт, шэеліт, апатыт, касітэрыт, вольфраміт, пірыт, сфалерыт, лазурыт, мускавіт, галеніт, халькапірыт, родохрозит, марганцевая руда, даламіт, каліевы палявы шпат, шпінель, барыт і інш. ва ўласцівасцях спадарожных мінералаў у флюорите, падзел і ачыстка ажыццяўляюцца шляхам флотации, магнітнай сепарацыі, гравітацыйнай сепарацыі і іншых метадаў ўзбагачэння.
①Флотацыя
Флотацыя - найважнейшы спосаб ўзбагачэння флюарыту. Агульны працэс заключаецца ў зборы тоўстых кіслот пасля драбнення і выбары кваліфікаваных флюарытавых канцэнтратаў праз некалькі працэсаў адбору; для звязаных сульфідных мінералаў выбіраюцца жоўтыя прэпараты, а звязаныя барыт, кальцыт, мускавіт і г.д. аддзяляюцца інгібітарамі.
②Перавыбранне – выпуск
Калі ўтрыманне руды нізкае або змяшчае шмат грубых злучаных тэл, звычайна выкарыстоўваецца камбінаваны працэс гравітацыйнага падзелу і флотации.
③ Магнітная сепарацыя – флотация
Калі ў рудзе шмат магнітнага жалеза або аксідаў жалеза, барабанны магнітны сепаратар можна выкарыстоўваць для аддзялення моцнага магнітнага жалеза або вертыкальны кальцавой магнітны сепаратар для выдалення слабамагнітнага аксіду жалеза і затым прайсці праз працэс флотации; калі ў зыходнай рудзе мала мінералаў жалеза, аднак, калі ўтрыманне жалеза ў флатарытавым канцэнтраце перавышае стандарт, для выдалення мінералаў аксіду жалеза з флюарытавага канцэнтрату шляхам моцнай магнітнай сепарацыі можна выкарыстоўваць вертыкальны кальцавой або электрамагнітны магнітны сепаратар з высокім градыентам, каб палепшыць якасць канцэнтрату.
Магнітны сепаратар з вертыкальным кальцавым высокаградыентным астуджэннем нафты і вады
Нізкотэмпературны звышправодны магнітны сепаратар
Барабанны магнітны сепаратар
Атрыманне плавікавай кіслаты
Плавікавая кіслата - асноўны хімічны прадукт. Плавікавая кіслата атрымліваецца шляхам раскладання флюарыту сернай кіслатой, так званым сернакіслотным спосабам. Ён надзвычай агрэсіўны і мае шырокі спектр прымянення. Ён часта выкарыстоўваецца для выдалення пяску ў металічных адлівах, выдалення графітавага попелу, ачысткі металу, вытворчасці паўправаднікоў, апрацоўкі керамікі, тручэння шкла, нафтавых каталізатараў і г.д.
Тэст на выдаленне флюорытавай руды
Утрыманне CaF2 у флюарытавым чарнавым канцэнтраце, атрыманым шляхам флотации рэдказямельных хвастоў у Баян-Обо, складае ўсяго 86,17 %, што значна адрозніваецца ад патрабаванняў да кваліфікаваных канцэнтратаў. Чарнавы канцэнтрат акрамя флюарыту змяшчае таксама рэдказямельныя рэчывы і гематыт. , ліманіт, кальцыт, апатыт, піраксен натрыю, амфібол, біятыт і іншыя мінералы. Зборшчыкі мыла тлустых кіслот, якія выкарыстоўваюцца пры флатацыі флюарыту, аказваюць пэўны эфект збору жалезазмяшчальных мінералаў. Сярод гэтых мінералаў-прымешак гематыт, ліманіт, піраксен натрыю, амфібол і біятыт слабамагнітныя і могуць быць выдалены з дапамогай моцнай магнітнай сепарацыі для паляпшэння якасці флюарытавага канцэнтрату.
Грубы канцэнтрат флюарыту -200 меш з тонкасцю 93,50% быў падвергнуты параўнальным выпрабаванням на выдаленне прымешак і ачыстку з дапамогай двух высокатрывалых працэсаў магнітнай сепарацыі, такіх як вертыкальнае кальцо + электрамагнітная суспензія, магнітны сепаратар з высокім градыентам і вертыкальнае кольца + звышправодны магнітны сепаратар .
Падчас параўнальнага тэсту на выдаленне моцных магнітных прымешак было выяўлена, што некаторыя мінералы, такія як гематыт, ліманіт і біятыт, з адносна высокай удзельнай магнітнай успрымальнасцю могуць быць эфектыўна выдалены моцным магнітным аддзяленнем вертыкальнага кольца, і марка CaF2 флюарыту канцэнтрат быў павялічаны з 86,17%. Затым жалезазмяшчальныя мінералы са слабымі магнітнымі ўласцівасцямі выдаляюцца з дапамогай электрамагнітнай суспензіі і звышправоднага магнітнага сепаратара, і ступень CaF2 у флюарытавым канцэнтраце павялічваецца да 93,84% і 95,63% адпаведна, абодва дасягаючы FC-93 і FC-95. стандарт якасці. Узбагачальны эфект высокаградыентнага магнітнага сепаратара з вертыкальным кольцам і электрамагнітнай суспензіяй і нізкатэмпературнага звышправоднага магнітнага сепаратара больш відавочны, што можа забяспечыць надзейную тэхнічную аснову для выдалення моцных магнітных прымешак і ачысткі такіх мінералаў.
Прыкладанні
Вертыкальны кальцавой высокаградыентны магнітны сепаратар выкарыстоўваецца ў праекце рэдказямельнай магнітнай сепарацыі ва Унутранай Манголіі
У праекце выкарыстоўваюцца два вертыкальныя кальцавыя магнітныя сепаратары з высокім градыентам 1,7 Т і адзін нізкатэмпературны звышправодны магнітны сепаратар 5,0 Т, якія могуць эфектыўна палепшыць якасць флюарытавага канцэнтрату, дасягнуць добрага аднаўлення рэдказямельных элементаў і павялічыць вытворчасць і эфектыўнасць.
Праект моцнай магнітнай сепарацыі па ўзбагачэнні рэдказямельных элементаў у правінцыі Сычуань. Праект выкарыстоўвае 8 камплектаў вертыкальных кальцавых высокаградыентных магнітных сепаратараў 1,4 Т для падзелу і аднаўлення рэдказямельных элементаў, і эфект добры.
Час размяшчэння: 6 мая 2022 г